Metabolismo

Estrutura do trifosfato de adenosina, um intermediário central no metabolismo energético.
Metabolismo (do grego metabolismos, μεταβολισμός, que significa "mudança", troca[1]) é o conjunto de transformações que as substâncias químicas sofrem no interior dos organismos vivos. A expressão metabolismo celular é usada em referência ao conjunto de todas as reações químicas que ocorrem nas células. Estas reacções são responsáveis pelos processos de síntese e degradação dos nutrientes na célula e constituem a base da vida, permitindo o crescimento e reprodução das células, mantendo as suas estruturas e adequando respostas aos seus ambientes.
As reações químicas do metabolismo estão organizadas em vias metabólicas, que são sequências de reacções em que o produto de uma reacção é utilizado como reagente na reacção seguinte. Diferentes enzimas catalisam diferentes passos de vias metabólicas, agindo de forma concertada de modo a não interromper o fluxo nessas vias. As enzimas são vitais para o metabolismo porque permitem a realização de reacções desejáveis mas termodinamicamente desfavoráveis, ao acoplá-las a reacções mais favoráveis. As enzimas regulam as vias metabólicas em resposta a mudanças no ambiente celular ou a sinais de outras células.
O metabolismo é normalmente dividido em dois grupos: anabolismo e catabolismo. Reacções anabólicas, ou reacções de síntese, são reacções químicas que produzem nova matéria orgânica nos seres vivos. Sintetizam-se novos compostos (moléculas mais complexas) a partir de moléculas simples (com consumo de energia sob a forma de ATP). Reacções catabólicas, ou reacções de decomposição/degradação, são reacções químicas que produzem grandes quantidades de energia (ATP) a partir da decomposição ou degradação de moléculas mais complexas (matéria orgânica). Quando o catabolismo supera em atividade o anabolismo, o organismo perde massa, o que acontece em períodos de jejum ou doença; mas se o anabolismo superar o catabolismo, o organismo cresce ou ganha massa. Se ambos os processos estão em equilíbrio, o organismo encontra-se em equilíbrio dinâmico ou homeostase. O metabolismo é fundamentalmente estudado pela Bioquímica, usando muitas vezes também técnicas ligadas à Biologia Molecular e à Genética.
Índice
1 Características gerais
2 História
3 Substâncias bioquímicas relevantes
3.1 Aminoácidos e proteínas
3.2 Lípidos
3.3 Glícidos
3.4 Ácidos nucleicos
3.5 Coenzimas
4 Minerais e cofactores
5 Catabolismo
5.1 Digestão
5.2 Energia de compostos orgânicos
5.3 Fosforilação oxidativa
5.4 Energia de compostos inorgânicos
5.5 Energia luminosa
6 Anabolismo
6.1 Fixação de carbono
6.2 Glícidos
6.3 Ácidos gordos, isoprenóides e esteróides
6.4 Proteínas
6.5 Síntese de nucleótidos
7 Metabolismo redox e de xenobióticos
8 Termodinâmica de sistemas vivos
9 Metabolismo e a temperatura
10 Regulação e controle
11 Evolução
12 Métodos de estudo
13 Referências
14 Bibliografia
15 Ver também
16 Ligações externas
Características gerais |
O metabolismo de um organismo determina quais substâncias são nutricionais e quais são tóxicas. Por exemplo, alguns procariontes utilizam ácido sulfídrico como nutriente; este gás é no entanto venenoso para animais.[2] A velocidade a que se processa o metabolismo, determinada pela taxa metabólica, também influencia a quantidade de alimento requerida por um organismo.
Uma característica do metabolismo é a semelhança de vias metabólicas básicas entre espécies muito diferentes. Por exemplo, o conjunto de intermediários reacionais encontrados no ciclo dos ácidos tricarboxílicos é encontrado de forma universal, em células tão diferentes como a bactéria Escherichia coli ou o elefante.[3] Esta estrutura metabólica semelhante está provavelmente associada à grande eficiência dessas vias e na sua antiguidade na história da evolução.[4][5]
História |

Santorio Santorio sentado na sua cadeira-balança. De Ars de statica medecina, publicado pela primeira vez em 1614.
A história do estudo científico do metabolismo estende-se por quatro séculos, tendo evoluído da observação de organismos animais inteiros até ao estudo de reacções metabólicas individuais na Bioquímica moderna. As primeiras experiências conduzidas de forma controlada foram publicadas por Santorio Santorio em 1614 no seu livro Ars de statica medecina.[6] Neste, Santorio descreveu como determinou o seu próprio peso antes e depois de comer, beber, dormir, trabalhar, ter relações sexuais, jejuar e excretar. Ele descobriu que a maior parte da comida ingerida era perdida no que ele chamou de "perspiração insensível".
Nestes estudos iniciais, os mecanismos destes processos metabólicos não eram conhecidos; pensava-se que o tecido vivo era animado por uma "força vital".[7]
No século XIX, enquanto estudava a fermentação do açúcar a álcool por leveduras, Louis Pasteur concluiu que a fermentação era catalisada por substâncias dentro das células de levedura, a que ele chamou de "fermentos". Pasteur escreveu que "a fermentação alcoólica é um acto correlacionado com a vida e organização das células de levedura, não com a morte ou putrefacção das células."
[8] Esta descoberta, junto com a publicação da síntese química da ureia por Friedrich Wöhler em 1828,[9] provou que os compostos orgânicos e as reacções químicas existentes nas células partilham o mesmo princípio que qualquer outra área da Química.
A descoberta das enzimas no início do século XX, por Eduard Buchner, separou o estudo das reacções químicas do metabolismo do estudo biológico das células, marcando o início da Bioquímica como ciência independente.[10] A quantidade de conhecimento bioquímico cresceu rapidamente durante o início do século XX. Um dos bioquímicos mais prolíficos dessa época foi Hans Krebs, que fez diversas contribuições no estudo do metabolismo.[11] Ele descobriu o ciclo da ureia e, mais tarde, junto com Hans Kornberg, o ciclo dos ácidos tricarboxílicos (também conhecido por esta razão como ciclo de Krebs) e o ciclo do glioxilato.[12][13]
A investigação bioquímica moderna tem sido ajudada com a invenção e desenvolvimento de diversas técnicas, como a cromatografia, a difracção de raios X, a espectroscopia de ressonância magnética nuclear, a marcação isotópica, a microscopia electrónica e simulações de dinâmica molecular. Estas técnicas permitiram a descoberta e análise detalhada de diversas moléculas e vias metabólicas nas células.
Substâncias bioquímicas relevantes |

Estrutura de um triacilglicerol.
A maioria das estruturas que compõem os seres vivos é fabricada a partir de três classes básicas de moléculas: aminoácidos, glícidos e lípidos. Como estas moléculas são vitais, o metabolismo concentra-se na fabricação destas, na construção de células e tecidos ou na sua degradação para uso como fonte de energia. Muitos compostos bioquímicos podem ser ligados entre si formando polímeros, como o ADN e as proteínas. Estas macromoléculas são parte essencial de todos os organismos vivos.
Alguns dos polímeros mais comuns estão listados abaixo:
| Tipo de molécula | Nome da forma monomérica | Nome da forma polimérica | Exemplos de formas poliméricas |
|---|---|---|---|
Aminoácidos | Aminoácidos | Proteínas (ou polipéptidos) | Proteínas fibrilares e proteínas globulares |
Glícidos | Monossacarídeos | Polissacarídeos | Amido, glicogénio e celulose |
Ácidos nucleicos | Nucleótidos | Polinucleótidos | ADN e ARN |
Aminoácidos e proteínas |
As proteínas são compostas por aminoácidos dispostos numa cadeia linear e ligados entre si por ligações peptídicas. Muitas proteínas são as enzimas que catalisam as reacções químicas no metabolismo. Outras proteínas têm funções estruturais ou mecânicas, como o sistema de armação celular usado para manter a forma da célula, o citoesqueleto.[14]
As proteínas têm também papéis importantes na sinalização celular, resposta imunitária, adesão celular, transporte activo através de membranas e no ciclo celular.[15]
Lípidos |
Os lípidos são o grupo mais diversificado de compostos bioquímicos. Constituem grande parte das membranas biológicas, tais como a membrana celular; além desta função estrutural, também servem como fonte de energia.[15] Os lípidos são normalmente definidos como moléculas biológicas hidrofóbicas ou anfipáticas solúveis em solventes orgânicos como o benzeno ou o clorofórmio.[16]
As gorduras são um grupo alargado de compostos que inclui os ácidos gordos e o glicerol; uma molécula de glicerol ligada a três ácidos gordos por uma ligação éster é um triacilglicerol.[17] Existem diversas variações desta estrutura básica, por exemplo a presença de esfingosina em esfingolípidos e grupos hidrofílicos como o fosfato nos fosfolípidos.
Os esteróides, como o colesterol, são outro grupo significativo de lípidos sintetizados em células.[18]
Glícidos |
Os glícidos são aldeídos ou cetonas contendo diversos grupos funcionais hidroxilo. Os glícidos simples podem existir numa forma linear ou numa forma cíclica. São as moléculas biológicas mais abundantes e possuem funções muito diversificadas, como o armazenamento e transporte de energia (sob a forma de amido e glicogénio) e construção de elementos estruturais (como a celulose em plantas e a quitina em animais).[15]

Estrutura da glicose convertida da projecção de Fisher (linear) para a de Haworth (cíclica).
Os glícidos mais simples são os monossacarídeos, que incluem a galactose, a frutose e a glicose. Os monossacarídeos podem formar polímeros designados polissacarídeos de formas muito diversas.[19]
Ácidos nucleicos |
Os polímeros ADN e ARN são longas cadeias de nucleótidos. Estas macromoléculas são essenciais no armazenamento e uso da informação genética, através dos processos de transcrição e síntese proteica.[15] Esta informação é protegida por mecanismos de reparação do ADN e propagada através da replicação do ADN. Alguns vírus têm um genoma constituído por ARN (por exemplo, o HIV), e usam transcrição reversa para sintetizar ADN a partir desse ARN.[20]
O ARN de ribozimas (como o spliceossoma) apresenta actividade enzimática tal como as enzimas proteicas, pois pode catalisar reacções químicas.
Os nucleósidos são sintetizados a partir da ligação de uma base azotada a uma ribose. Estas bases são anéis heterocíclicos contendo azoto, classificados como purinas ou pirimidinas. Os nucleótidos também actuam como coenzimas em reacções de transferência de grupos químicos.[21]
Coenzimas |

Estrutura da coenzima acetil-CoA. O grupo acetilo encontra-se ligado ao átomo de enxofre, na extremidade esquerda.
O metabolismo envolve um vasto conjunto de reacções químicas, mas a maioria cai dentro de alguns tipos básicos de transferências de grupos funcionais.[22] Esta química comum permite às células usarem um conjunto relativamente pequeno de intermediários metabólicos no transporte de grupos químicos de uma reacção para a seguinte.[21] Estes intermediários de transferência de grupos são as coenzimas. Cada classe de reacção de transferência de grupos corresponde a uma determinada coenzima, servindo de substrato para um conjunto de enzimas que a produz e que a consome. Assim, as coenzimas são continuamente produzidas, consumidas e então recicladas.[23]
A coenzima mais central é o trifosfato de adenosina (ATP), a moeda de troca energética universal das células. O ATP é utilizado para transferir energia química entre diferentes reacções químicas. Existe uma pequena quantidade de ATP permanentemente presente nas células, mas como é constantemente regenerado, o corpo humano é capaz de utilizar o seu peso em ATP por dia.[23] O ATP age como uma ponte entre catabolismo e anabolismo, tendo as reacções catabólicas como produtoras de ATP e as anabólicas como consumidoras. Também serve como um transportador de grupos fosfato em reacções de fosforilação.
As vitaminas são compostos orgânicos necessários em pequenas quantidades e que não podem ser sintetizados pelas células. Na nutrição humana, a maioria das vitaminas funciona como coenzimas após sofrerem uma modificação química; por exemplo, todas as vitaminas hidrossolúveis são fosforiladas ou ligadas a nucleótidos para a sua utilização intracelular.[24] O dinucleótido de nicotinamida-adenina (NADH), um derivado da vitamina B3 (niacina), é uma coenzima importante que age como aceitador de hidrogénio. Centenas de diferentes tipos de desidrogenases retiram electrões dos seus substratos e reduzem NAD+ a NADH. Esta forma reduzida da coenzima é então substrato para redutases celulares que necessitem de reduzir os seus substratos.[25] O dinucleótido de nicotinamida-adenina existe também sob uma forma fosfatada, NADPH. O par redox NAD+/NADH é mais importante no catabolismo, enquanto que o par NADP+/NADPH é mais usado no anabolismo.
Minerais e cofactores |

Estrutura da hemoglobina (PDB 1GZX). As subunidades da proteínas encontram-se coloridas a vermelho e azul, encontrando-se os grupos hemo a verde.
Cerca de 99% da massa dos mamíferos é constituída pelos elementos carbono, azoto, hidrogénio, oxigénio, cálcio, magnésio, sódio, potássio, cloro e enxofre.[26] Destes, são considerados "inorgânicos" os metais, o enxofre e o cloro. Enquanto que alguns dos elementos inorgânicos são abundantes em sistemas vivos (como o sódio e o potássio), outros encontram-se em quantidades vestigiais. Os compostos orgânicos (proteínas, lípidos, glícidos) contêm a maioria do carbono e azoto; a maioria do oxigénio e hidrogénio encontra-se sob a forma de água.[26]
Os elementos inorgânicos mais abundantes actuam como electrólitos. Os iões mais importantes são o sódio, potássio, cálcio, magnésio, cloreto, fosfato e o ião orgânico bicarbonato. A existência de gradientes iónicos através de membranas celulares mantém a pressão osmótica e o pH.[27] Os iões são também vitais para nervos e músculos, pois os potenciais de acção usados nestes tecidos são produzidos através da troca de electrólitos entre o fluido extracelular e o citoplasma.[28] Os electrólitos entram e saem das células através de proteínas transmembranares denominadas canais iónicos. Por exemplo, a contracção muscular depende do movimento de cálcio, sódio e potássio através de canais iónicos na membrana celular e túbulos-T.[29]
Os metais de transição são normalmente elementos vestigiais em organismos, sendo o zinco e o ferro os mais abundantes.[30][31] Estes metais são usados por algumas proteínas como cofactores e são essenciais para a actividade de metaloenzimas como a catalase e proteínas de transporte de dioxigénio como a hemoglobina.[32] Tais metais actuam como cofactores quer estando ligados directamente à cadeia polipeptídica, quer estejam integrados em moléculas orgânicas complexas que por sua vez se encontram ligadas à cadeia polipeptídica. Os cofactores sofrem modificações durante a catálise enzimática mas voltam sempre ao seu estado inicial no fim de um ciclo catalítico. Os metais de transição são absorvidos pelos organismos usando transportadores específicos e ligam-se a proteínas de armazenamento como a ferritina e a metalotioneína quando não é necessária a sua disponibilidade para intervir no metabolismo.[33][34]
Catabolismo |
O catabolismo é o conjunto das reacções metabólicas que libertam energia. Tais reacções incluem a degradação e oxidação de moléculas encontradas em alimentos, assim como reacções que captam a energia luminosa da luz solar. As reacções catabólicas providenciam energia e componentes necessários às reacções anabólicas. A natureza exacta destas reacções catabólicas difere de organismo para organismo: organismos organotróficos usam moléculas orgânicas como fonte de energia, enquanto litotróficos usam substratos inorgânicos e fototróficos captam energia solar, transformando-a em energia química.
Todas estas diferentes formas de metabolismo dependem de reacções redox que envolvem a transferência de electrões de moléculas doadoras reduzidas, como moléculas orgânicas, água, amoníaco, ácido sulfídrico ous iões ferrosos (Fe2+), para moléculas aceitadoras, como o dioxigénio (O2), o nitrato (NO3−) ou o sulfato (SO42-).[35] Em animais, estas reacções envolvem a degradação de moléculas orgânicas complexas a moléculas mais simples, como dióxido de carbono (CO2) e água (H2O). Em organismos fotossintéticos, como as plantas e cianobactérias, estas reacções de transferência electrónica não libertam energia, sendo antes utilizadas como forma de armazenar energia absorvida da luz solar.[36]
O conjunto de reacções catabólicas mais comum em animais pode ser separado em três etapas diferentes. Na primeira etapa, moléculas orgânicas complexas como as proteínas, polissacarídeos ou lípidos são degradados nos seus componentes fora das células. Na etapa seguinte, estas moléculas de menor tamanho são importadas pelas células e convertidas a moléculas menores, normalmente o acetil-CoA, num processo que liberta energia. Na última etapa, o grupo acetilo do acetil-CoA é oxidado a água e dióxido de carbono, libertando energia que é armazenada através da redução da coenzima dinucleótido de nicotinamida-adenina, NAD+, a NADH.

Um esquema simplificado do catabolismo de proteínas, polissacarídeos e lípidos.
Digestão |
Macromoléculas como o amido ou as proteínas não podem ser rapidamente assimilados pelas células, tendo de ser degradados nos seus componentes de menor tamanho antes de poderem ser utilizados no metabolismo celular. A digestão destes polímeros é feita por diversas classes de enzimas. Estas enzimas digestivas incluem as proteases, que digerem proteínas a aminoácidos, e glicosídeo hidrolases, que digerem polissacarídeos a monossacarídeos.
Os microorganismos excretam enzimas digestivas para o ambiente ao seu redor,[37][38] enquanto que os animais segregam estas enzimas em células especializadas do sistema digestivo.[39] Os aminoácidos ou açúcares libertados por estas enzimas extracelulares são então assimiladas pelas células através de proteínas específicas usando transporte activo.[40][41]
Energia de compostos orgânicos |
O catabolismo de glícidos consiste na degradação de glícidos complexos em unidades de menor tamanho. Os glícidos são normalmente assimilados pelas células após a sua digestão a monossacarídeos.[42] Após entrada na célula, a principal via de degradação é a glicólise, em que açúcares como a glucose e a frutose são convertidos a piruvato, com formação em simultâneo de ATP.[43] O piruvato é um intermediáro de diversas vias metabólicas, mas a maioria é convertida a acetil-CoA, que entra no ciclo dos ácidos tricarboxílicos (ciclo de Krebs). Embora haja mais alguma formação de ATP neste ciclo, o produto principal deste é o NADH, resultante da redução do NAD+ quando o acetil-CoA é oxidado. Esta oxidação liberta dióxido de carbono (CO2). Uma via alternativa de degradação da glicose é a Via das pentoses-fosfato, que reduz a coenzima NADPH e produz pentoses como a ribose, o açúcar componente dos ácidos nucleicos.
As gorduras são catabolizadas por hidrólise a ácidos gordos livres e glicerol. O glicerol entra na glicólise e os ácidos gordos são degradados por beta-oxidação a acetil-CoA, que entra então no ciclo dos ácidos tricarboxílicos. Devido à sua grande proporção de grupos metileno e pelo facto de os glícidos possuirem mais oxigénio nas suas estruturas químicas, os ácidos gordos libertam mais energia que os glícidos quando oxidados.
Os aminoácidos são utilizados na síntese de proteínas e outras biomoléculas, ou oxidados a ureia e dióxido de carbono para obtenção de energia.[44] A via de oxidação começa com a remoção do grupo amina por uma transaminase, deixando um esqueleto de carbono sob a forma de um cetoácido; o grupo amina é então metabolizado no ciclo da ureia. Vários cetoácidos obtidos através da desaminação de aminoácidos são também intermediários no ciclo dos ácidos tricarboxílicos: por exemplo, a desaminação do glutamato forma α-cetoglutarato.[45] Os aminoácidos glucogénicos também podem ser convertidos a glicose, através da gluconeogénese.[46]
Fosforilação oxidativa |
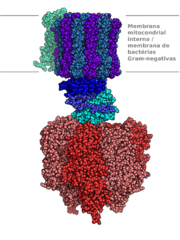
Estrutura da ATP sintase. O canal de protões encontra-se a azul e a subunidade com actividade de sintase a vermelho.
Na fosforilação oxidativa, os electrões obtidos na oxidação de moléculas em diversas vias metabólicas, como por exemplo o ciclo dos ácidos tricarboxílicos, são transferidos para o dioxigénio, e a energia libertada é usada na produção de ATP. Em eucariontes, este processo é feito por uma série de proteínas, a cadeia de transporte electrónico, que se encontram nas membranas mitocondriais. Em procariontes, estas proteínas encontram-se na membrana celular interna.[47] Estas proteínas utilizam a energia obtida da oxidação de NADH para transportar protões através da membrana.[48]
O transporte de protões para o exterior da mitocôndria cria uma diferença de concentração de protões entre os dois compartimentos, criando um gradiente electroquímico.[49] A presença deste gradiente força os protões a regressarem ao interior da mitocôndria através da ATP sintase. O fluxo de protões provoca a rotação da subunidade inferior da ATP sintase, o que causa a fosforilação de difosfato de adenosina (ADP) a trifosfato de adenosina (ATP).[23]
Energia de compostos inorgânicos |
A quimiolitotrofia é um tipo de metabolismo encontrado em procariontes, em que a energia é obtida a partir da oxidação de compostos inorgânicos. Estes organismos podem usar hidrogénio,[50] compostos reduzidos de enxofre (como sulfuretos, ácido sulfídrico e tiossulfato),[2]óxidos de ferro (II),[51] ou amoníaco[52] como fontes de agentes redutores, ganhando energia a partir da oxidação destes compostos com aceitadores de electrões como o oxigénio ou o nitrito.[53] Estes processos microbiológicos são importantes em ciclos biogeoquímicos como a acetogénese, a nitrificação e a desnitrificação e são de importância crítica para a fertilidade do solo.[54][55]
Energia luminosa |
A energia da luz solar é captada por plantas, cianobactérias, alguns tipos de bactérias e de protistas. Este processo está frequentemente associado à fixação de dióxido de carbono em compostos orgânicos, que é um processo integrante da fotossíntese. Os sistemas de captura de energia e de fixação de carbono podem trabalhar separadamente em procariontes, como acontece com as bactérias púrpura e as bactérias verdes sulfurosas. Estas bactérias usam a luz solar como fonte de energia mas alternam o seu metabolismo entre a fixação de carbono e a fermentação de compostos orgânicos.[56][57]
A captação de energia solar é um processo semelhante à fosforilação oxidativa, pois ambos os processos envolvem o armazenamento de energia sob a forma de um gradiente de protões, que leva à síntese de ATP.[23] No caso da fotossíntese, os electrões necessários para o funcionamento da cadeia de transporte electrónico provêm de proteínas colectoras de luz denominadas centros reaccionais fotossintéticos. Estas estruturas dividem-se em dois tipos dependendo do pigmento fotossintético presente; a maioria das bactéria fotossintéticas possui apenas um tipo de centro, enquanto as plantas e as cianobactérias possuem dois.[58]
Em plantas, o fotossistema II usa energia luminosa para remover electrões da água, libertando oxigénio no processo. Os electrões movem-se então para o complexo do citocromo b6f, que usa a sua energia para transportar protões através das membranas dos tilacóides nos cloroplastos.[15] Estes protões regressam ao interior dos tilacóides através da ATP sintase, num processo semelhante ao descrito nas mitocôndrias. Estes electrões podem então entrar no fotossistema I e ser utilizados na redução de NADP+, no ciclo de Calvin ou reciclados para gerar ainda mais ATP.[59]
Anabolismo |
O anabolismo é o conjunto de reacções metabólicas de síntese em que a energia libertada pelo catabolismo é utilizada para construir moléculas complexas. Em geral, as moléculas complexas que constituem estruturas celulares são construídas passo a passo a partir de precursores mais simples. O anabolismo divide-se em três etapas fundamentais:
- a síntese de precursores como aminoácidos, monossacarídeos, isoprenóides e nucleótidos,
- a activação destes precursores a formas reactivas usando energia proveniente do ATP
- e finalmente a construção de moléculas complexas, tais como proteínas, polissacarídeos, lípidos e ácidos nucleicos, a partir destes precursores activados.
Os organismos diferem entre si na quantidade de diferentes moléculas que conseguem sintetizar. Os seres autotróficos, como as plantas, podem construir moléculas complexas (polissacarídeos e proteínas) a partir de moléculas muito simples como o dióxido de carbono e a água. Os seres heterotróficos necessitam de fontes alimentares para providenciar monossacarídeos e aminoácidos, para poder produzir macromoléculas. Os organismos podem ainda ser classificados segundo a fonte primária da sua energia: fotoautotróficos e foto-heterotróficos obtém energia a partir da luz solar, enquanto que organismos quimioautotróficos e quimio-heterotróficos obtêm energia a partir de reacções de oxidação.
Fixação de carbono |

Células vegetais apresentando cloroplastos (a verde), que são os organelos em que ocorre a fotossíntese.
A fotossíntese é o processo em que ocorre síntese de glicose a partir da luz solar, dióxido de carbono e água, havendo produção de oxigénio. Este processo utiliza ATP e NADPH produzido pelos centros reaccionais fotossintéticos para converter CO2 em glicerol-3-fosfato, que pode ser então convertido a glicose. Esta reacção de fixação de carbono é catalisada pela enzima RuBisCO e é parte integrante do ciclo de Calvin.[60] Ocorrem três tipos de fotossíntese em plantas: fixação de carbono em plantas C3, fixação de carbono em plantas C4 e fotossíntese CAM. Estes tipos de fotossíntese diferem na via que o CO2 toma até ao ciclo de Calvin: as plantas C3 fixam o CO2 directamente, enquanto que as C4 e CAM incorporam-no noutros compostos de forma a adaptar a condições de alta luminosidade e dessecação.[61] Algas e plantas aquáticas usam organelas chamadas pirenóides.
Os mecanismos de fixação de carbono em procariontes fotossintéticos são mais diversificados. O CO2 pode ser fixado através do ciclo de Calvin, de um ciclo dos ácidos tricarboxílicos inverso[62] ou através da carboxilação do acetil-CoA.[63][64] Procariontes quimioautotróficos também utilizam o ciclo de Calvin para a fixação de carbono mas a energia usada nas reacções provém de compostos inorgânicos.[65]
Glícidos |
No anabolismo de glícidos, ácidos orgânicos simples podem ser convertidos a monossacarídeos como a glicose, sendo então usados para sintetizar polissacarídeos como o amido. A produção de glicose a partir de compostos como o piruvato, o lactato, o glicerol, o glicerol-3-fosfato e aminoácidos é chamada gluconeogénese. Na gluconeogénese, o piruvato é convertido a glicose-6-fosfato usando diversos intermediários, muitos deles comuns à glicólise.[43] No entanto, esta via não se resume a uma inversão da glicólise, pois diversos passos são catalisados por enzimas não-glicolíticas. Este é um aspecto importante pois permite a regulação separada da formação e da degradação da glicose, evitando que ambas as vias funcionem em simultâneo num ciclo fútil.[66][67]
Embora a gordura seja um modo comum de armazenamento de energia, em vertebrados, como os humanos, os ácidos gordos não podem ser convertidos a glicose através da gluconeogénese, pois estes organismos são incapazes de transformar acetil-CoA em piruvato.[68] Por essa razão, após um longo jejum os vertebrados necessitam de produzir corpos cetónicos a partir de ácidos gordos para substituir a glicose em falta em tecidos e órgãos que não conseguem metabolizar ácidos gordos, como o cérebro.[69] Noutros organismos, como plantas e bactérias, este problema metabólico é ultrapassado utilizando o ciclo do glioxilato, que evita o passo de descarboxilação no ciclo dos ácidos tricarboxílicos e permite a transformação de acetil-CoA a oxaloacetato, que pode ser então utilizado na produção de glicose.[13][68]
Os polissacarídeos e os glicanos são sintetizados através da adição sequencial de monossacarídeos, catalisada por glicosiltransferases, de um doador de açúcar fosforilado como o difosfato de uridina-glicose (UDP-glicose) para um grupo hidroxilo aceitador no polissacarídeo nascente. Como qualquer um dos grupos hidroxilo da estrutura do substrato podem ser aceitadores, os polissacarídeos podem ter estruturas lineares ou ramificadas.[70]
Os polissacarídeos podem desempenhar funções estruturais ou metabólicas, podendo também ser transferidos para lípidos e proteínas pelas enzimas oligossacariltransferases.[71][72]
Ácidos gordos, isoprenóides e esteróides |

Esquema simplificado da via de síntese de esteróides, mostrando os intermediários metabólicos pirofosfato de isopentenilo (IPP), pirofosfato de dimetilalilo (DMAPP), pirofosfato de geranilo (GPP) e esqualeno. Outros intermediários foram omitidos para maior claridade.
Os ácidos gordos são sintetizados pelas sintases de ácido gordo, que polimerizam e reduzem unidades de acetil-CoA. As cadeias acilo dos ácidos gordos são aumentadas através de um ciclo de reacções que adicionam o grupo acilo, reduzem-no à forma álcool, desidratam este a um grupo alceno, sendo este finalmente reduzido a um grupo alcano. As enzimas envolvidas na biossíntese de ácidos gordos encontram-se divididas em dois grupos: em animais e fungos todas estas reacções são catalisadas por uma proteína multifuncional (tipo I),[73] enquanto que em plantas e bactérias diferentes enzimas catalisam as diversas reacções (tipo II).[74][75]
Os terpenos e os isoprenoides são uma classe de lípidos, que inclui os carotenóides, sendo a maior classe de produtos naturais vegetais.[76] Estes compostos são sintetizados através da montagem e modificação de unidades de isopreno doadas pelas moléculas precursoras pirofosfato de isopentenilo e pirofosfato de dimetilalilo.[77] Estes precursores podem ser obtidos de diferentes formas. Em animais e arqueas, a via do mevalonato produz estes compostos a partir do acetil-CoA,[78] enquanto que plantas e bactérias existe uma via alternativa (do não-mevalonato) que utiliza piruvato e 3-fosfato de gliceraldeído como substratos.[77][79]
Uma reacção importante que utiliza estes doadores de isopreno é a síntese de esteróides. Nesta, as unidades de isopreno são unidas formando esqualeno; este é então convertido a lanosterol.[80] O lanosterol pode ser então convertido a outros esteróides, como o colesterol e o ergosterol.[80][81]
Proteínas |
Diferentes organismos possuem diferentes capacidades de sintetizar os vinte aminoácidos mais comuns. A maioria das bactérias e plantas conseguem sintetizar todos os vinte aminoácidos; os mamíferos conseguem sintetizar apenas dez, denominados não-essenciais por esta razão.[15] Assim, os aminoácidos essenciais têm de ser obtidos através da alimentação. Todos os aminoácidos são sintetizados a partir de intermediários da glicólise, do ciclo dos ácidos tricarboxílicos ou da via das pentoses-fosfato; o azoto não existente nestes intermediários é fornecido pelo glutamato ou pela glutamina. A síntese dos aminoácidos depende da formação do alfa-cetoácido apropriado, que sofre então transaminação para formar um aminoácido.[82]
Os aminoácidos são utilizados na síntese de proteínas, ao serem ligados entre si por ligações peptídicas numa cadeia linear. Os aminoácidos podem ser ligados num número de combinações quase infinito, fazendo com que cada proteína tenha uma sequência única de aminoácidos, denominada estrutura primária. As proteínas são sintetizadas a partir de aminoácidos activados através de uma ligação éster a uma molécula de ARN de transferência (ARNt ou tRNA). Estes aminoácidos activados, os aminoacil-tRNA, são sintetizados pela aminoacil-tRNA sintetase, numa reacção dependente da presença de ATP.[83] Os ribossomas actuam então no aminoacil-tRNA, agregando-o à cadeia polipeptídica nascente, segundo a informação dada pelo ARN mensageiro.[84]
Síntese de nucleótidos |
Os nucleótidos são sintetizados a partir de aminoácidos, dióxido de carbono e ácido fórmico em vias metabólicas que necessitam de grandes quantidades de energia.[85] As purinas são sintetizadas a partir de nucleósidos (bases ligadas à ribose). Tanto a adenina como a guanina são sintetizadas a partir do monofosfato de inosina, que por sua vez é sintetizado usando átomos provenientes dos aminoácidos glicina, glutamina e aspartato, assim como de formato transferido pela coenzima tetra-hidrofolato. As pirimidinas são sintetizadas a partir da base orotato, formada a partir da glutamina e do aspartato.[86]
Metabolismo redox e de xenobióticos |
Todos os organismos são constantemente expostos a compostos que não podem ser utilizados no metabolismo normal e que são potencialmente tóxicos se se acumularem nas células. Tais compostos são designados xenobióticos.[87] Os xenobióticos, incluindo substâncias como drogas sintéticas, venenos e antibióticos, são desintoxicados usando um conjunto de enzimas específicas. Em humanos, estas enzimas incluem as citocromo P450 oxidases,[88] as UDP-glucuronosiltransferases[89] e as glutationo-S-transferases.[90]
Este sistema de enzimas actua em três fases. Na fase I, o xenobiótico é oxidado; na fase II, existe conjugação de grupos hidrofílicos no xenobiótico oxidado, de modo a torná-lo mais hidrossolúvel; na fase III, o xenobiótico modificado é expulso das células, podendo sofrer mais algum metabolismo em organismos multicelulares antes da sua excreção. Estas reacções são bastante importantes em termos ecológicos, nomeadamente na biodegradação microbiana de agentes poluentes e biorremediação de terras contaminadas e derrames de combustíveis.[91]
Muitas destas reacções microbianas são idênticas às existentes em organismos multicelulares. No entanto, e graças à sua enorme diversidade, os microorganismos conseguem desintoxicar uma variedade superior de xenobióticos que os organismos multicelulares, conseguindo inclusivamente degradar agentes poluentes orgânicos persistentes, como compostos organoclorados.[92]
Um problema relacionado com o dos xenobióticos prende-se com a existência de stress oxidativo em organismos aeróbios.[93] Os processos associados à vida em aerobiose, como a fosforilação oxidativa e a formação de ligações dissulfureto em proteínas, produzem espécies reactivas de oxigénio, como o peróxido de hidrogénio.[94] Estas espécies danosas são removidas por antioxidantes, como a glutationa, e enzimas, como a catalase e outras peroxidases.[95][96]
Termodinâmica de sistemas vivos |
Os sistemas vivos têm de obedecer às leis da termodinâmica. A grande complexidade dos organismos aparentemente contradiz a segunda lei da termodinâmica, que enuncia que a entropia de um sistema fechado tende a aumentar; no entanto, os sistemas vivos são sistemas abertos que trocam energia e massa com o seu exterior. Assim, os organismos não se encontram em equilíbrio termodinâmico, sendo antes sistemas dissipativos, pois mantêm a sua ordem ao aumentar a entropia do seu ambiente.[97] O metabolismo celular faz a ponte entre o processo espontâneo de catabolismo e o processo não espontâneo de anabolismo para obter este efeito. Em termos termodinâmicos, o metabolismo mantém a ordem ao criar desordem.[98]
Metabolismo e a temperatura |
Em fungos, bactérias, plantas ou animais de sangue quente ou frio, vários processos interagem com a temperatura interna e externa aos organismos. As plantas e leveduras parecem ter um termostato biológico simples. Na planta Arabidopsis thaliana, uma única proteína (a histona H2A) desempenha o papel em variações de temperatura inferiores a 1° C. Esta proteína altera o enrolamento do DNA, controlando assim o acesso a determinadas moléculas de DNA, ou inibindo a ativação de genes. Este efeito de "bio-termostato" parece ser comum na natureza. Entender esses mecanismos também pode ajudar a compreender melhor alguns dos efeitos da mudança do clima. [99][100]
Regulação e controle |
O ambiente da maioria dos organismos encontra-se em constante mudança, sendo necessária uma apertada regulação das reacções metabólicas de modo a manter um conjunto de condições mais ou menos constante nas células, chamado homeostase.[101][102] A regulação metabólica permite aos organismos dar resposta a estímulos do exterior, permitindo a interacção com o seu ambiente.[103] Existem dois conceitos relacionados que são importantes para a compreensão da forma como são reguladas vias metabólicas: em primeiro lugar, a regulação de uma enzima numa via refere-se ao aumento ou diminuição da sua actividade enzimática em resposta a estímulos; o segundo conceito é o controlo exercido por esta enzima na velocidade total da via por sofrer variações na sua actividade enzimática, ou seja, o controlo do fluxo da via metabólica.[104] Por exemplo, uma enzima pode sofrer grandes alterações na sua actividade (ou seja, ser muito regulada) mas se estas mudanças não tiverem um efeito significativo no fluxo da via metabólica, então esta enzima não está envolvida no controlo da via.[105]

Efeito da insulina na absorção e metabolismo da glicose. A insulina liga-se ao seu receptor (1) que por sua vez inicia diversas cascatas de sinalização (2) tais como a translocação do transportador Glut-4 para a membrana plasmática e entrada de glicose (3), síntese de glicogénio (4), glicólise (5) e síntese de ácidos gordos (6).
Existem diversos níveis de regulação metabólica. Na regulação intrínseca, a via metabólica regula-se a si própria em resposta a mudanças nos níveis de substratos ou produtos; por exemplo, uma diminuição na quantidade de produto pode aumentar o fluxo da via para compensar essa diminuição.[104][106] Este tipo de regulação envolve frequentemente o uso de regulação alostérica das diversas enzimas que participam na via metabólica. O controlo extrínseco corresponde à mudança do metabolismo de uma célula num organismo multicelular em resposta a sinais de outras células. Estes sinais são normalmente moléculas mensageiras solúveis, como hormonas e factores de crescimento, e são detectados por receptores específicos na superfície das células.[107] Tais sinais são então transmitidos para o interior da célula por sistemas de mensageiros secundários que envolvem frequentemente a fosforilação de proteínas.[108]
A regulação do metabolismo da glicose pela insulina é um exemplo bem conhecido de controlo extrínseco.[109] A insulina é produzida em resposta a um aumento da glicemia. A ligação da hormona a receptores de insulina na superfície de células activa uma cascata de cinases que provoca a absorção de glicose pelas células e a sua conversão a moléculas de armazenamento, como o glicogénio e os ácidos gordos.[110] O metabolismo do glicogénio é controlado pela actividade da glicogénio fosforilase, a enzima que hidrolisa o glicogénio, e pela glicogénio sintase, a enzima que o sintetiza. Estas enzimas são reguladas de forma recíproca, em que a fosforilação activa a fosforilase e inibe a sintase. A insulina provoca a síntese de glicogénio ao activar fosfatases, produzindo um decréscimo na fosforilação destas enzimas.[111]
Evolução |

A árvore filogenética, mostrando as relações entre organismos decorrentes da evolução das espécies. A azul: bactérias; a verde: arqueas; a vermelho: eucariotas. São também mostradas as posições relativas de alguns filos.
As vias metabólicas descritas acima são comuns aos três domínios da vida (Eukarya, Archaea e Bacteria), considerando-se por isso que estavam também presentes no mais recente antecessor comum aos três domínios.[3][112] Este antecessor era procariótico e provavelmente metanogénico, possuindo um extenso metabolismo de lípidos, aminoácidos, nucleótidos e glícidos.[113] A preservação destas vias durante a evolução que se seguiu poderá ter resultado de serem uma solução optimizada para os seus problemas metabólicos específicos: ocorre a produção de metabolitos de forma eficiente e com um número mínimo de passos reaccionais.[4][5]
Diversos são os modelos propostos para a descrição da evolução de novas vias metabólicas, incluindo a adição sequencial de enzimas a curtas vias ancestrais, a duplicação e posterior divergência evolutiva de vias metabólicas inteiras e a inclusão de enzimas pré-existentes numa nova via reaccional.[114] Não é clara a importância relativa destes mecanismos, mas diversos estudos genómicos sugerem que as enzimas de uma dada via metabólica possuem um antecessor comum. Esta ancestralidade comum implica que diversas vias terão evoluído passo a passo, com a criação de novas funções a partir de passos reaccionais pré-existentes.[115] Existe também a possibilidade de que partes do metabolismo existam como "módulos" que podem ser reutilizados em diferentes vias e que desempenham funções semelhantes em diferentes moléculas.[116]
A evolução de organismos pode levar também à perda de vias metabólicas. Por exemplo, em alguns parasitas, processos metabólicos que não são essenciais à sua sobrevivência são perdidos; o parasita absorve então aminoácidos, nucleótidos e glícidos do seu hospedeiro.[117] Organismos endossimbióticos apresentam também capacidades metabólicas similarmente reduzidas.[118]
Métodos de estudo |
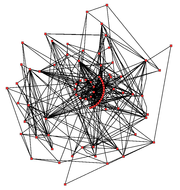
Rede metabólica do ciclo dos ácidos tricarboxílicos de Arabidopsis thaliana. As enzimas e os metabolitos encontram-se representados com quadrados vermelhos e as suas interacções com traços pretos.
O metabolismo é classicamente estudado usando uma aproximação reducionista, focando uma via metabólica isoladamente. A marcação isotópica de precursores é de grande utilidade em estudos com organismos inteiros, tecidos ou células, pois permite seguir o percurso dessas moléculas até serem transformadas no produto final, analisando intermediários e produtos marcados radioactivamente.[119] As enzimas que catalisam estas reacções podem ser purificadas e analisadas do ponto de vista da sua actividade enzimática, medindo parâmetros cinéticos e respostas a inibidores. Outro tipo de investigação consiste na identificação de metabolitos numa célula ou tecido; o conjunto de metabolitos é por vezes designado metaboloma. De uma forma geral, este tipo de estudos é adequado para alcançar uma visão geral de uma via metabólica simples, mas é limitado quando aplicado a sistemas mais complexos, como o funcionamento de uma célula inteira.[120]
É possível ter uma ideia da complexidade da rede metabólica existente nas células, que possuem tipicamente milhares de enzimas, analisando a figura ao lado, que representa apenas 43 proteínas e 40 metabolitos. A sequenciação de genomas mostra que poderão existir até 45000 genes (que corresponderão a tantos outros polipéptidos).[121] É, no entanto, possível usar esta informação genómica para reconstruir redes completas de reacções bioquímicas e produzir modelos matemáticos holísticos que expliquem e prevejam o seu comportamento.[122] Tais modelos são particularmente úteis quando usados na integração de dados obtidos através de métodos laboratoriais de análise de expressão genética, como o uso de proteómica e microarrays.[123]
Uma relevante aplicação tecnológica desta informação é a engenharia metabólica, em que organismos como leveduras, plantas ou bactérias são geneticamente modificados de modo a serem úteis em aplicações biotecnológicas, como a produção de medicamentos (por exemplo, antibióticos) ou reagentes químicos (como o propan-1,3-diol ou o ácido xiquímico).[124]
Referências
↑ «Metabolism». The Online Etymology Dictionary. Consultado em 20 de fevereiro de 2007
↑ ab Friedrich C (1998). «Physiology and genetics of sulfur-oxidizing bacteria». Adv Microb Physiol. 39: 235-89. PMID 9328649
↑ ab Smith E, Morowitz H (2004). «Universality in intermediary metabolism». Proc Natl Acad Sci U S A. 101 (36): 13168-73. PMID 15340153
↑ ab Ebenhöh O, Heinrich R (2001). «Evolutionary optimization of metabolic pathways. Theoretical reconstruction of the stoichiometry of ATP and NADH producing systems». Bull Math Biol. 63 (1): 21–55. PMID 11146883
↑ ab Meléndez-Hevia E, Waddell T, Cascante M (1996). «The puzzle of the Krebs citric acid cycle: assembling the pieces of chemically feasible reactions, and opportunism in the design of metabolic pathways during evolution». J Mol Evol. 43 (3): 293–303. PMID 8703096 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Eknoyan G (1999). «Santorio Sanctorius (1561–1636) - founding father of metabolic balance studies». Am J Nephrol. 19 (2): 226-33. PMID 10213823
↑ Williams, H. S. (1904) A History of Science: in Five Volumes. Volume IV: Modern Development of the Chemical and Biological Sciences Harper and Brothers (New York) Retrieved on 2007-03-26
↑ Dubos J. (1951). «Louis Pasteur: Free Lance of Science, Gollancz. Quoted in Manchester K. L. (1995) Louis Pasteur (1822 – 1895)—chance and the prepared mind.». Trends Biotechnol. 13 (12): 511–515. PMID 8595136
↑ Kinne-Saffran E, Kinne R (1999). «Vitalism and synthesis of urea. From Friedrich Wöhler to Hans A. Krebs». Am J Nephrol. 19 (2): 290-4. PMID 10213830
↑ Eduard Buchner's 1907 Nobel lecture at http://nobelprize.org Accessed 2007-03-20
↑ Kornberg H (2000). «Krebs and his trinity of cycles». Nat Rev Mol Cell Biol. 1 (3): 225-8. PMID 11252898
↑ Krebs H A, Henseleit K (1932) "Untersuchungen über die Harnstoffbildung im tierkorper." Z. Physiol. Chem. 210, 33 – 66. Krebs H, Johnson W (1937). = pubmed&pubmedid = 16746382 «Metabolism of ketonic acids in animal tissues» Verifique valor|url=(ajuda). Biochem J. 31 (4): 645-60. PMID 16746382
↑ ab Kornberg H, Krebs H (1957). «Synthesis of cell constituents from C2-units by a modified tricarboxylic acid cycle». Nature. 179 (4568): 988-91. PMID 13430766
↑ Michie K, Löwe J (2006). «Dynamic filaments of the bacterial cytoskeleton». Annu Rev Biochem. 75: 467-92. PMID 16756499
↑ abcdef David L. Nelson; Michael M. Cox (2005). Lehninger Principles of Biochemistry. New York: W. H. Freeman and company. 841 páginas. ISBN 0-7167-4339-6 A referência emprega parâmetros obsoletos|coautores=(ajuda)
↑ Fahy E, Subramaniam S, Brown H, Glass C, Merrill A, Murphy R, Raetz C, Russell D, Seyama Y, Shaw W, Shimizu T, Spener F, van Meer G, VanNieuwenhze M, White S, Witztum J, Dennis E (2005). «A comprehensive classification system for lipids». J Lipid Res. 46 (5): 839-61. PMID 15722563 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ «Nomenclature of Lipids». IUPAC-IUB Commission on Biochemical Nomenclature (CBN). Consultado em 8 de março de 2007
↑ Hegardt F (1999). = 1220089&blobtype = pdf «Mitochondrial 3-hydroxy-3-methylglutaryl-CoA synthase: a control enzyme in ketogenesis» Verifique valor|url=(ajuda). Biochem J. 338 (Pt 3): 569-82. PMID 10051425
↑ Raman R, Raguram S, Venkataraman G, Paulson J, Sasisekharan R (2005). «Glycomics: an integrated systems approach to structure-function relationships of glycans». Nat Methods. 2 (11): 817-24. PMID 16278650 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Sierra S, Kupfer B, Kaiser R (2005). «Basics of the virology of HIV-1 and its replication». J Clin Virol. 34 (4): 233-44. PMID 16198625 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ ab Wimmer M, Rose I (1978). «Mechanisms of enzyme-catalyzed group transfer reactions». Annu Rev Biochem. 47: 1031–78. PMID 354490
↑ Mitchell P (1979). «The Ninth Sir Hans Krebs Lecture. Compartmentation and communication in living systems. Ligand conduction: a general catalytic principle in chemical, osmotic and chemiosmotic reaction systems». Eur J Biochem. 95 (1): 1–20. PMID 378655
↑ abcd Dimroth P, von Ballmoos C, Meier T (2006). = pubmed&pubmedid = 16607397 «Catalytic and mechanical cycles in F-ATP synthases. Fourth in the Cycles Review Series» Verifique valor|url=(ajuda). EMBO Rep. 7 (3): 276-82. PMID 16607397 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Ann Coulston; John Kerner, JoAnn Hattner, Ashini Srivastava (2006). «Nutrition Principles and Clinical Nutrition». Stanford School of Medicine Nutrition Courses. [S.l.]: SUMMIT A referência emprega parâmetros obsoletos|coautores=(ajuda)
↑ Pollak N, Dölle C, Ziegler M (2007). «The power to reduce: pyridine nucleotides—small molecules with a multitude of functions». Biochem J. 402 (2): 205-18. PMID 17295611 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ ab Heymsfield S, Waki M, Kehayias J, Lichtman S, Dilmanian F, Kamen Y, Wang J, Pierson R (1991). «Chemical and elemental analysis of humans in vivo using improved body composition models». Am J Physiol. 261 (2 Pt 1): E190-8. PMID 1872381 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Sychrová H (2004). «Yeast as a model organism to study transport and homeostasis of alkali metal cations» (PDF). Physiol Res. 53 Suppl 1: S91-8. PMID 15119939
↑ Levitan I (1988). «Modulation of ion channels in neurons and other cells». Annu Rev Neurosci. 11: 119-36. PMID 2452594
↑ Dulhunty A (2006). «Excitation-contraction coupling from the 1950s into the new millennium». Clin Exp Pharmacol Physiol. 33 (9): 763-72. PMID 16922804
↑ Mahan D, Shields R (1998). «Macro- and micromineral composition of pigs from birth to 145 kilograms of body weight». J Anim Sci. 76 (2): 506-12. PMID 9498359
↑ Husted S, Mikkelsen B, Jensen J, Nielsen N (2004). «Elemental fingerprint analysis of barley (Hordeum vulgare) using inductively coupled plasma mass spectrometry, isotope-ratio mass spectrometry, and multivariate statistics». Anal Bioanal Chem. 378 (1): 171-82. PMID 14551660 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Finney L, O'Halloran T (2003). «Transition metal speciation in the cell: insights from the chemistry of metal ion receptors». Science. 300 (5621): 931-6. PMID 12738850
↑ Cousins R, Liuzzi J, Lichten L (2006). «Mammalian zinc transport, trafficking, and signals». J Biol Chem. 281 (34): 24085-9. PMID 16793761 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Dunn L, Rahmanto Y, Richardson D (2007). «Iron uptake and metabolism in the new millennium». Trends Cell Biol. 17 (2): 93–100. PMID 17194590 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Nealson K, Conrad P (1999). = pubmed&pubmedid = 10670014 «Life: past, present and future» Verifique valor|url=(ajuda). Philos Trans R Soc Lond B Biol Sci. 354 (1392): 1923–39. PMID 10670014
↑ Nelson N, Ben-Shem A (2004). «The complex architecture of oxygenic photosynthesis». Nat Rev Mol Cell Biol. 5 (12): 971-82. PMID 15573135
↑ Häse C, Finkelstein R (1993). = pubmed&pubmedid = 8302217 «Bacterial extracellular zinc-containing metalloproteases» Verifique valor|url=(ajuda). Microbiol Rev. 57 (4): 823-37. PMID 8302217
↑ Gupta R, Gupta N, Rathi P (2004). «Bacterial lipases: an overview of production, purification and biochemical properties». Appl Microbiol Biotechnol. 64 (6): 763-81. PMID 14966663 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Hoyle T (1997). «The digestive system: linking theory and practice». Br J Nurs. 6 (22): 1285–91. PMID 9470654
↑ Souba W, Pacitti A (1992). «How amino acids get into cells: mechanisms, models, menus, and mediators». JPEN J Parenter Enteral Nutr. 16 (6): 569-78. PMID 1494216
↑ Barrett M, Walmsley A, Gould G (1999). «Structure and function of facilitative sugar transporters». Curr Opin Cell Biol. 11 (4): 496–502. PMID 10449337 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Bell G, Burant C, Takeda J, Gould G (1993). «Structure and function of mammalian facilitative sugar transporters». J Biol Chem. 268 (26): 19161-4. PMID 8366068 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ ab Bouché C, Serdy S, Kahn C, Goldfine A (2004). «The cellular fate of glucose and its relevance in type 2 diabetes». Endocr Rev. 25 (5): 807-30. PMID 15466941 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Sakami W, Harrington H (1963). «Amino acid metabolism». Annu Rev Biochem. 32: 355-98. PMID 14144484
↑ Brosnan J (2000). «Glutamate, at the interface between amino acid and carbohydrate metabolism». J Nutr. 130 (4S Suppl): 988S-90S. PMID 10736367
↑ Young V, Ajami A (2001). «Glutamine: the emperor or his clothes?». J Nutr. 131 (9 Suppl): 2449S-59S; discussion 2486S-7S. PMID 11533293
↑ Hosler J, Ferguson-Miller S, Mills D (2006). «Energy transduction: proton transfer through the respiratory complexes». Annu Rev Biochem. 75: 165-87. PMID 16756489 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Schultz B, Chan S (2001). «Structures and proton-pumping strategies of mitochondrial respiratory enzymes». Annu Rev Biophys Biomol Struct. 30: 23–65. PMID 11340051
↑ Capaldi R, Aggeler R (2002). «Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor». Trends Biochem Sci. 27 (3): 154-60. PMID 11893513
↑ Friedrich B, Schwartz E (1993). «Molecular biology of hydrogen utilization in aerobic chemolithotrophs». Annu Rev Microbiol. 47: 351-83. PMID 8257102
↑ Weber K, Achenbach L, Coates J (2006). «Microorganisms pumping iron: anaerobic microbial iron oxidation and reduction». Nat Rev Microbiol. 4 (10): 752-64. PMID 16980937 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Jetten M, Strous M, van de Pas-Schoonen K, Schalk J, van Dongen U, van de Graaf A, Logemann S, Muyzer G, van Loosdrecht M, Kuenen J (1998). «The anaerobic oxidation of ammonium». FEMS Microbiol Rev. 22 (5): 421-37. PMID 9990725 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Simon J (2002). «Enzymology and bioenergetics of respiratory nitrite ammonification». FEMS Microbiol Rev. 26 (3): 285–309. PMID 12165429
↑ Conrad R (1996). = pubmed&pubmedid = 8987358 «Soil microorganisms as controllers of atmospheric trace gases (H2, CO, CH4, OCS, N2O, and NO)» Verifique valor|url=(ajuda). Microbiol Rev. 60 (4): 609-40. PMID 8987358
↑ Barea J, Pozo M, Azcón R, Azcón-Aguilar C (2005). «Microbial co-operation in the rhizosphere». J Exp Bot. 56 (417): 1761–78. PMID 15911555 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ van der Meer M, Schouten S, Bateson M, Nübel U, Wieland A, Kühl M, de Leeuw J, Sinninghe Damsté J, Ward D (2005). = pubmed&pubmedid = 16000812 «Diel variations in carbon metabolism by green nonsulfur-like bacteria in alkaline siliceous hot spring microbial mats from Yellowstone National Park» Verifique valor|url=(ajuda). Appl Environ Microbiol. 71 (7): 3978–86. PMID 16000812 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Tichi M, Tabita F (2001). = pubmed&pubmedid = 11591679 «Interactive control of Rhodobacter capsulatus redox-balancing systems during phototrophic metabolism» Verifique valor|url=(ajuda). J Bacteriol. 183 (21): 6344–54. PMID 11591679
↑ Allen J, Williams J (1998). «Photosynthetic reaction centers». FEBS Lett. 438 (1–2): 5–9. PMID 9821949
↑ Munekage Y, Hashimoto M, Miyake C, Tomizawa K, Endo T, Tasaka M, Shikanai T (2004). «Cyclic electron flow around photosystem I is essential for photosynthesis». Nature. 429 (6991): 579-82. PMID 15175756 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Miziorko H, Lorimer G (1983). «Ribulose-1,5-bisphosphate carboxylase-oxygenase». Annu Rev Biochem. 52: 507-35. PMID 6351728
↑ Dodd A, Borland A, Haslam R, Griffiths H, Maxwell K (2002). «Crassulacean acid metabolism: plastic, fantastic». J Exp Bot. 53 (369): 569-80. PMID 11886877 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Hügler M, Wirsen C, Fuchs G, Taylor C, Sievert S (2005). = pubmed&pubmedid = 15838028 «Evidence for autotrophic CO2 fixation via the reductive tricarboxylic acid cycle by members of the epsilon subdivision of proteobacteria» Verifique valor|url=(ajuda). J Bacteriol. 187 (9): 3020–7. PMID 15838028 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Strauss G, Fuchs G (1993). «Enzymes of a novel autotrophic CO2 fixation pathway in the phototrophic bacterium Chloroflexus aurantiacus, the 3-hydroxypropionate cycle». Eur J Biochem. 215 (3): 633-43. PMID 8354269
↑ Wood H (1991). «Life with CO or CO2 and H2 as a source of carbon and energy». FASEB J. 5 (2): 156-63. PMID 1900793
↑ Shively J, van Keulen G, Meijer W (1998). «Something from almost nothing: carbon dioxide fixation in chemoautotrophs». Annu Rev Microbiol. 52: 191–230. PMID 9891798 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Boiteux A, Hess B (1981). «Design of glycolysis». Philos Trans R Soc Lond B Biol Sci. 293 (1063): 5–22. PMID 6115423
↑ Pilkis S, el-Maghrabi M, Claus T (1990). «Fructose-2,6-bisphosphate in control of hepatic gluconeogenesis. From metabolites to molecular genetics». Diabetes Care. 13 (6): 582-99. PMID 2162755 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ ab Ensign S (2006). «Revisiting the glyoxylate cycle: alternate pathways for microbial acetate assimilation». Mol Microbiol. 61 (2): 274-6. PMID 16856935
↑ Finn P, Dice J. «Proteolytic and lipolytic responses to starvation». Nutrition. 22 (7–8): 830-44. PMID 16815497
↑ Rademacher T, Parekh R, Dwek R (1988). «Glycobiology». Annu Rev Biochem. 57: 785–838. PMID 3052290 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Opdenakker G, Rudd P, Ponting C, Dwek R (1993). «Concepts and principles of glycobiology». FASEB J. 7 (14): 1330–7. PMID 8224606 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ McConville M, Menon A (2000). «Recent developments in the cell biology and biochemistry of glycosylphosphatidylinositol lipids (review)». Mol Membr Biol. 17 (1): 1–16. PMID 10824734
↑ Chirala S, Wakil S (2004). «Structure and function of animal fatty acid synthase». Lipids. 39 (11): 1045–53. PMID 15726818
↑ White S, Zheng J, Zhang Y (2005). «The structural biology of type II fatty acid biosynthesis». Annu Rev Biochem. 74: 791–831. PMID 15952903 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Ohlrogge J, Jaworski J (1997). «Regulation of fatty acid synthesis». Annu Rev Plant Physiol Plant Mol Biol. 48: 109–136. PMID 15012259
↑ Dubey V, Bhalla R, Luthra R (2003). «An overview of the non-mevalonate pathway for terpenoid biosynthesis in plants» (PDF). J Biosci. 28 (5): 637-46. PMID 14517367 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ ab Kuzuyama T, Seto H (2003). «Diversity of the biosynthesis of the isoprene units». Nat Prod Rep. 20 (2): 171-83. PMID 12735695
↑ Grochowski L, Xu H, White R (2006). = pubmed&pubmedid = 16621811 «Methanocaldococcus jannaschii uses a modified mevalonate pathway for biosynthesis of isopentenyl diphosphate» Verifique valor|url=(ajuda). J Bacteriol. 188 (9): 3192–8. PMID 16621811 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Lichtenthaler H (1999). «The 1-Ddeoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants». Annu Rev Plant Physiol Plant Mol Biol. 50: 47–65. PMID 15012203
↑ ab Schroepfer G (1981). «Sterol biosynthesis». Annu Rev Biochem. 50: 585–621. PMID 7023367
↑ Lees N, Skaggs B, Kirsch D, Bard M (1995). «Cloning of the late genes in the ergosterol biosynthetic pathway of Saccharomyces cerevisiae—a review». Lipids. 30 (3): 221-6. PMID 7791529 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Arthur C. Guyton; John E. Hall (2006). Textbook of Medical Physiology. Philadelphia: Elsevier. pp. 855–6. ISBN 0-7216-0240-1 A referência emprega parâmetros obsoletos|coautores=(ajuda)
↑ Ibba M, Söll D (2001). «The renaissance of aminoacyl-tRNA synthesis». EMBO Rep. 2 (5): 382-7. PMID 11375928
↑ Lengyel P, Söll D (1969). = 378322&blobtype = pdf «Mechanism of protein biosynthesis» Verifique valor|url=(ajuda). Bacteriol Rev. 33 (2): 264–301. PMID 4896351
↑ Rudolph F (1994). «The biochemistry and physiology of nucleotides». J Nutr. 124 (1 Suppl): 124S-127S. PMID 8283301 Zrenner R, Stitt M, Sonnewald U, Boldt R (2006). «Pyrimidine and purine biosynthesis and degradation in plants». Annu Rev Plant Biol. 57: 805-36. PMID 16669783 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Smith J (1995). «Enzymes of nucleotide synthesis». Curr Opin Struct Biol. 5 (6): 752-7. PMID 8749362
↑ Testa B, Krämer S (2006). «The biochemistry of drug metabolism—an introduction: part 1. Principles and overview». Chem Biodivers. 3 (10): 1053-101. PMID 17193224
↑ Danielson P (2002). «The cytochrome P450 superfamily: biochemistry, evolution and drug metabolism in humans». Curr Drug Metab. 3 (6): 561-97. PMID 12369887
↑ King C, Rios G, Green M, Tephly T (2000). «UDP-glucuronosyltransferases». Curr Drug Metab. 1 (2): 143-61. PMID 11465080 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Sheehan D, Meade G, Foley V, Dowd C (2001). = pubmed&pubmedid = 11695986 «Structure, function and evolution of glutathione transferases: implications for classification of non-mammalian members of an ancient enzyme superfamily» Verifique valor|url=(ajuda). Biochem J. 360 (Pt 1): 1–16. PMID 11695986 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Galvão T, Mohn W, de Lorenzo V (2005). «Exploring the microbial biodegradation and biotransformation gene pool». Trends Biotechnol. 23 (10): 497–506. PMID 16125262 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Janssen D, Dinkla I, Poelarends G, Terpstra P (2005). «Bacterial degradation of xenobiotic compounds: evolution and distribution of novel enzyme activities». Environ Microbiol. 7 (12): 1868–82. PMID 16309386 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Davies K (1995). «Oxidative stress: the paradox of aerobic life». Biochem Soc Symp. 61: 1–31. PMID 8660387
↑ Tu B, Weissman J (2004). «Oxidative protein folding in eukaryotes: mechanisms and consequences». J Cell Biol. 164 (3): 341-6. PMID 14757749
↑ Sies H (1997). «Oxidative stress: oxidants and antioxidants» (PDF). Exp Physiol. 82 (2): 291-5. PMID 9129943
↑ Vertuani S, Angusti A, Manfredini S (2004). «The antioxidants and pro-antioxidants network: an overview». Curr Pharm Des. 10 (14): 1677–94. PMID 15134565 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ von Stockar U, Liu J (1999). «Does microbial life always feed on negative entropy? Thermodynamic analysis of microbial growth». Biochim Biophys Acta. 1412 (3): 191–211. PMID 10482783
↑ Demirel Y, Sandler S (2002). «Thermodynamics and bioenergetics». Biophys Chem. 97 (2–3): 87–111. PMID 12050002
↑ Brown JH, Gillooly JF, Allen AP, Savage VM, West GB (2004) Rumo a uma teoria metabólica da ecologia. Ecology, 85, 1771-1789
↑ Nicholson JK, Lindon JC, E. Holmes 'Metabonomics': compreensão das respostas metabólicas dos sistemas vivos a estímulos fisiopatológicos através de análise estatística multivariada de dados espectroscópicos de RMN. Xenobiotica 1999, 29: 1181-9
↑ Albert R (2005). «Scale-free networks in cell biology». J Cell Sci. 118 (Pt 21): 4947–57. PMID 16254242
↑ Brand M (1997). «Regulation analysis of energy metabolism». J Exp Biol. 200 (Pt 2): 193–202. PMID 9050227
↑ Soyer O, Salathé M, Bonhoeffer S (2006). «Signal transduction networks: topology, response and biochemical processes». J Theor Biol. 238 (2): 416-25. PMID 16045939 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ ab Salter M, Knowles R, Pogson C (1994). «Metabolic control». Essays Biochem. 28: 1–12. PMID 7925313 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Westerhoff H, Groen A, Wanders R (1984). «Modern theories of metabolic control and their applications (review)». Biosci Rep. 4 (1): 1–22. PMID 6365197 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Fell D, Thomas S (1995). = pubmed&pubmedid = 7575476 «Physiological control of metabolic flux: the requirement for multisite modulation» Verifique valor|url=(ajuda). Biochem J. 311 (Pt 1): 35-9. PMID 7575476
↑ Hendrickson W (2005). «Transduction of biochemical signals across cell membranes». Q Rev Biophys. 38 (4): 321-30. PMID 16600054
↑ Cohen P (2000). «The regulation of protein function by multisite phosphorylation—a 25 year update». Trends Biochem Sci. 25 (12): 596–601. PMID 11116185
↑ Lienhard G, Slot J, James D, Mueckler M (1992). «How cells absorb glucose». Sci Am. 266 (1): 86–91. PMID 1734513 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Roach P (2002). «Glycogen and its metabolism». Curr Mol Med. 2 (2): 101-20. PMID 11949930
↑ Newgard C, Brady M, O'Doherty R, Saltiel A (2000). «Organizing glucose disposal: emerging roles of the glycogen targeting subunits of protein phosphatase-1» (PDF). Diabetes. 49 (12): 1967–77. PMID 11117996 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Romano A, Conway T. «Evolution of carbohydrate metabolic pathways». Res Microbiol. 147 (6–7): 448-55. PMID 9084754
↑ Koch A (1998). «How did bacteria come to be?». Adv Microb Physiol. 40: 353-99. PMID 9889982 Ouzounis C, Kyrpides N (1996). «The emergence of major cellular processes in evolution». FEBS Lett. 390 (2): 119-23. PMID 8706840
↑ Schmidt S, Sunyaev S, Bork P, Dandekar T (2003). «Metabolites: a helping hand for pathway evolution?». Trends Biochem Sci. 28 (6): 336-41. PMID 12826406 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Light S, Kraulis P. «Network analysis of metabolic enzyme evolution in Escherichia coli». BMC Bioinformatics. 5. 15 páginas. PMID 15113413 Alves R, Chaleil R, Sternberg M (2002). «Evolution of enzymes in metabolism: a network perspective». J Mol Biol. 320 (4): 751-70. PMID 12095253 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Spirin V, Gelfand M, Mironov A, Mirny L (2006). = pubmed&pubmedid = 16731630 «A metabolic network in the evolutionary context: multiscale structure and modularity» Verifique valor|url=(ajuda). Proc Natl Acad Sci U S A. 103 (23): 8774–9. PMID 16731630 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Lawrence J (2005). «Common themes in the genome strategies of pathogens». Curr Opin Genet Dev. 15 (6): 584-8. PMID 16188434 Wernegreen J (2005). «For better or worse: genomic consequences of intracellular mutualism and parasitism». Curr Opin Genet Dev. 15 (6): 572-83. PMID 16230003
↑ Pál C, Papp B, Lercher M, Csermely P, Oliver S, Hurst L (2006). «Chance and necessity in the evolution of minimal metabolic networks». Nature. 440 (7084): 667-70. PMID 16572170 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Rennie M (1999). «An introduction to the use of tracers in nutrition and metabolism». Proc Nutr Soc. 58 (4): 935-44. PMID 10817161
↑ Phair R (1997). «Development of kinetic models in the nonlinear world of molecular cell biology». Metabolism. 46 (12): 1489–95. PMID 9439549
↑ Sterck L, Rombauts S, Vandepoele K, Rouzé P, Van de Peer Y (2007). «How many genes are there in plants (… and why are they there)?». Curr Opin Plant Biol. 10 (2): 199–203. PMID 17289424 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Borodina I, Nielsen J (2005). «From genomes to in silico cells via metabolic networks». Curr Opin Biotechnol. 16 (3): 350-5. PMID 15961036
↑ Gianchandani E, Brautigan D, Papin J (2006). «Systems analyses characterize integrated functions of biochemical networks». Trends Biochem Sci. 31 (5): 284-91. PMID 16616498 !CS1 manut: Nomes múltiplos: lista de autores (link)
↑ Thykaer J, Nielsen J (2003). «Metabolic engineering of beta-lactam production». Metab Eng. 5 (1): 56–69. PMID 12749845
González-Pajuelo M, Meynial-Salles I, Mendes F, Andrade J, Vasconcelos I, Soucaille P. «Metabolic engineering of Clostridium acetobutylicum for the industrial production of 1,3-propanediol from glycerol». Metab Eng. 7 (5–6): 329-36. PMID 16095939 !CS1 manut: Nomes múltiplos: lista de autores (link)
Krämer M, Bongaerts J, Bovenberg R, Kremer S, Müller U, Orf S, Wubbolts M, Raeven L (2003). «Metabolic engineering for microbial production of shikimic acid». Metab Eng. 5 (4): 277-83. PMID 14642355 !CS1 manut: Nomes múltiplos: lista de autores (link)
Bibliografia |
Nível introdutório
- Rose, S. and Mileusnic, R., The Chemistry of Life. (Penguin Press Science, 1999), ISBN 0-14-027273-9
- Schneider, E. D. and Sagan, D., Into the Cool: Energy Flow, Thermodynamics, and Life. (University Of Chicago Press, 2005), ISBN 0-226-73936-8
- Lane, N., Oxygen: The Molecule that Made the World. (Oxford University Press, USA, 2004), ISBN 0-19-860783-0
Nível avançado
- Price, N. and Stevens, L., Fundamentals of Enzymology: Cell and Molecular Biology of Catalytic Proteins. (Oxford University Press, 1999), ISBN 0-19-850229-X
- Berg, J. Tymoczko, J. and Stryer, L., Biochemistry. (W. H. Freeman and Company, 2002), ISBN 0-7167-4955-6
- Cox, M. and Nelson, D. L., Lehninger Principles of Biochemistry. (Palgrave Macmillan, 2004), ISBN 0-7167-4339-6
- Brock, T. D. Madigan, M. T. Martinko, J. and Parker J., Brock's Biology of Microorganisms. (Benjamin Cummings, 2002), ISBN 0-13-066271-2
- Da Silva, J.J.R.F. and Williams, R. J. P., The Biological Chemistry of the Elements: The Inorganic Chemistry of Life. (Clarendon Press, 1991), ISBN 0-19-855598-9
- Nicholls, D. G. and Ferguson, S. J., Bioenergetics. (Academic Press Inc., 2002), ISBN 0-12-518121-3
Ver também |
- Regulação do ciclo do ácido cítrico
- Regulação alostérica
- Biofísica
- Fermentação
- Calorimetria
- Ciclos da natureza
- NC-IUBMB
Ligações externas |
A Wikipédia tem o portal:
|
Informação geral
Esquema interactivo das principais vias metabólicas (em português)- Metabolismo, respiração celular e fotossíntese
- A bioquímica do metabolismo
- Ferramentas educativas interactivas
- Metabolismo microbiano
- Representações gráficas das principais vias metabólicas
- Química para biólogos
- Notas sobre bioquímica
- Guia de biologia molecular
- Artigo sobre metabolismo na Encyclopœdia Britannica
- Calcule sua taxa metabólica (equação de Harris-Benedict)
Glossários e dicionários
- Glossário de termos bioquímicos
- Glossário de termos bioquímicos
- Dicionário de biologia online
Metabolismo humano
- Tópicos em bioquímica moderna
- THE Medical Biochemistry Page
Bases de dados
- Esquema de vias metabólicas
- Base de dados KEGG PATHWAY
- Mapa das vias metabólicas IUBMB-Nicholson
- Reactome
Vias metabólicas
- Guia da glicólise
- O ciclo do azoto e fixação do azoto
- Guia da fotossíntese
- O que é a fotossíntese? Colecção de artigos e outros recursos
- O metabolismo das plantas